Целью разработки является создание экспериментального образца для переработки урины в водород.
Актуальность работы обеспечена следующими факторами:
1)Важной проблемой современной водородной энергетики являются способы хранения, транспортировки и синтеза водорода, так как многие из существующих способов синтеза энергозатратные и дорогие.
2)Используемое вещество для получения топлива является дешевым и экологически чистым, поэтому полученный водород будет экологически чистым.
Считается, что сам газ водород — экологичный и практичный источник энергии, потому что при его сгорании образуется только вода. Одной из важнейших проблем современной водородной энергетики являются способы хранения, транспортировки и генерации водорода. Многие из существующих способов энергозатратные и дорогие. Одной из основных проблем водородного аккумулирования электроэнергии является проблема организации компактной и безопасной системы хранения водорода в условиях окружающей среды.
Для решения поставленных задач использовались следующие методы исследования : сбор материала, анализ литературы, обработка информации, эксперимент, сравнение, анализ и обобщение результатов.
В ходе работы были выполнены все поставленные задачи, проверено и описано техническое решение, которое сможет обеспечить повышение надежности электропитания оборудования и снизить экологическую нагрузку на природу за счет применения водородных технологий, создан экспериментальный образец для переработки урины в водород.
Ключевые слова: хранение водорода, водородная энергетика, переработка отходов, получение водорода, водород, электролиз, урина.
Введение.
Водородная энергетика является одной из ведущих технологий для развития экономики, использование водорода в качестве основного или дополнительного энергоносителя является основной целью этой отрасли. Считается, что сам газ водород — экологичный и практичный источник энергии, потому что при его сгорании образуется только вода.
Актуальность работы обеспечена следующими факторами:
1) Важной проблемой современной водородной энергетики являются способы хранения, транспортировки и синтеза водорода, так как многие из существующих способов синтеза энергозатратные и дорогие.
2) Используемое вещество для получения топлива является дешевым и экологически чистым, поэтому полученный водород будет экологически чистым.
В предшествующей работе: «Urea electrolysis: direct hydrogen production from urine» (перевод: «Электролиз мочевины: прямое производство водорода из мочи»), авторы работы: Bryan K. Boggs, Rebecca L. King и Gerardine G. Botte, упоминается об использовании метода электролиза урины, где электроды выполнены из никеля, при напряжении 0,37 В [1].
Объект исследования: система утилизации отходов и переработки в энергию.
Предмет исследования: урина.
Гипотеза: возможно получение водорода из урины окажется выгодным и уместным в энергетике.
Цель: собрать экспериментальный образец для переработки урины в водород.
Задача: проверить способ получения водорода из урины.
Для решения поставленных задач использовались следующие методы исследования : сбор материала, анализ литературы, обработка информации, эксперимент, сравнение, анализ и обобщение результатов.
Технология получения водорода.
3.1 Аммиак образуется в виде отходов из многих естественных и лабораторных реакций. Аммиак можно выделить из урины, которая образуется в почках и выводит из организма лишнюю воду, соли, конечные продукты распада белков и другое, то есть урина является электролитом, это свойство понадобится в дальнейшем.
Разложение урины на водород электролизом. [2]
Для получения водорода был взят образец урины и для выделения из него аммиака проведен процесс гидролиза, который заключается в добавлении воды в нужное вещество в течение 30 минут [3]. Урина в результате реакции распалась на другие сложные вещества, об этом можно судить по изменению цвета раствора. В результате этого процесса жидкость приобрела темный цвет, образовался аммиак.
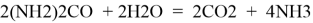
Измерим pH показатель урины, было получено следующее значение (pH = 5,78) и ее электропроводность (S = 11406 мкСм). Значение pH соответствует кислой среде, то есть концентрация ионов водорода высокая. После измерения был собран стенд для электролиза жидкости: стеклянный мерный стакан, два электрода, клеммы, лабораторный блок питания.
В качестве катода выступал свинец, анода — олово. Данное сочетание материалов обосновано их стоимостью и популярностью. Напряжение установлено на отметке 1,2 В, сила тока 1,2 А [4]. Процесс запустился, об этом говорит бурное протекание реакции: образование пузырьков газа на катоде и образование белого осадка на аноде (Sn(OH) 2 ) гидроксид олова. Также помимо гидроксида олова на аноде образуется азот.
Уравнения реакции на электродах:
на катоде:
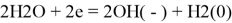
на аноде:
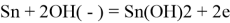
Именно из-за присутствия мочевины [5] в урине [6] при ее электролизе выделяется в 2 раза больше водорода чем при электролизе воды, потому что в одной молекуле мочевины содержится 4 атома водорода, а в 1 молекуле воды 2 атома. Для высвобождения водорода из урины потребуется меньшее количество энергии, потому что связь между атомами азота и водорода менее полярна, чем в молекуле воды между кислородом и водородом.
После завершения процесса (время эксперимента составило 20 секунд) жидкость стала темнее, что свидетельствует о протекании электролиза и предположительно переходе азота в другое состояние. При электролизе использовался раствор урины после гидролиза.
Повторно были произведены измерения значений pH и электропроводимости [7]. Значение pH увеличилось (pH = 9,13), среда из кислой стала щелочной. Электропроводность увеличилась (S = 12217 мкСм). Увеличение pH говорит об уменьшении ионов водорода, их высвобождении и образовании молекулы водорода. Электропроводность свидетельствует об увеличении концентрации солей в жидкости, ускорении процесса диссоциации. Для определения наличия водорода к поверхности жидкости был поднесен источник огня (спичка), в следствие раздался хлопок, характерный для сгорания водорода. Начальный объем жидкости составлял 40 мл вместе с электродом, после завершения процесса объем составил 37 мл вместе с электродом, то есть за 20 секунд 3 мл жидкости разложились на гидроксид олова на аноде и водород на катоде. На графиках представлены средние значения соответственные отрезку времени от 10 до 30 секунд.
3.2 Сравнение с существующими аналогами. В результате проведенного анализа научных публикаций, была найдена одна работа, проведенная американскими исследователями [1]. В данной работе использовался метод электролиза урины, электроды выполнены из никеля, а напряжение 0,37 В. Сравнивая мою методику с данной, электроды в моем случае выполнены из более дешевого материала, но напряжение у меня получилось большее. В дальнейшем планируется провести исследование в сфере электродов, для определения и разработки оптимального материала для электролиза мочи с минимальным напряжением.
Заключение.
В ходе работы были выполнены все поставленные цели и задачи: удалось собрать экспериментальный образец для переработки урины в водород и получить водород из урины.
Была проверена и описана технология электролиза.
Из-за присутствия мочевины в урине при ее электролизе выделяется в 2 раза больше водорода чем при электролизе воды. Поэтому можно использовать урину в качестве сырья для получения водорода.
Литература:
- Упоминание темы работы (https://pubs.rsc.org/en/content/articlelanding/2009/CC/b905974a);
- Электролиз (https://chemege.ru/electrolysis/);
- Процесс гидролиза (https://ru.wikipedia.org/wiki/Гидролиз);
- Учеб. пособие для хим.-тех. спец. вузов/ Под ред. К. С. Краснова. — М.: Высш. школа, 1982. -687 с. (С. 454–460)
- Мочевина (https://ru.wikipedia.org/wiki/Мочевина);
- Урина (https://ru.wikipedia.org/wiki/Моча);
- Курс общей химии./Коровин Н. В., Масленникова Г. Н., Гуськова Л. Г. и др. Под ред. Коровина Н. В. — М.: Высш. школа, 1981.











