Патофизиология МДД: ген DMD и дистрофин. Ген DMD — один из крупнейшихгенов в геноме человека, содержащий 79 экзонов и охватывающий более 2,6 млн пар оснований. Он отвечает за синтез белка дистрофина, представленного различными изоформами [2]. Из-за значительных размеров DMD особенно подвержен мутациям, среди которых наиболее распространены делеции (60 %), дупликации (6 %), а также точечные мутации и транслокации. Эти генетические изменения могут нарушать рамку считывания, что приводит к синтезу укороченных или нефункциональных форм дистрофина [2].
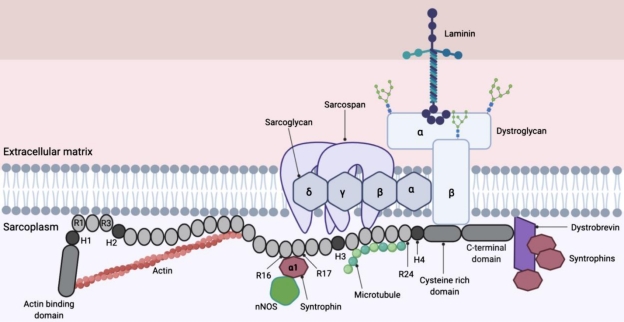
Основная изоформа дистрофина в скелетных и сердечных мышцах представляет собой цитоплазматический сарколеммальный белок массой 427 kD, который играет ключевую роль в связывании внеклеточного матрикса с кортикальным цитоскелетом [3]. Дистрофин широко экспрессируется в скелетных, сердечных и гладких мышцах, а также в ограниченном количестве присутствует в центральной нервной системе (ЦНС) [4,5]. В сарколемме он стабилизируется за счёт взаимодействия с комплексом белков, ассоцированных с дистрофином (DAPC) (см. рис. 1) [3].
Генная терапия при лечении МДД. Генная терапия рассматривается как одно из наиболее перспективных направлений в лечении МДД, так как направлена на устранение первопричины заболевания — мутаций в гене DMD. В настоящее время разрабатывается несколько стратегий, направленных на восстановление экспрессии дистрофина в мышечных клетках. Рассмотрим основные подходы:
- Методы доставки генетического материала. Для доставки терапевтических генов при лечении МДД используются различные векторные системы. Аденоассоциированные вирусы (AAV) являются наиболее распространёнными вирусными векторами благодаря их способности эффективно проникать в мышечные клетки и обеспечивать длительную экспрессию введённого гена DMD. Альтернативно, невирусные методы, такие как липосомы и наночастицы, предлагают возможность доставки генетического материала без использования вирусов, что снижает риск иммунных реакций, но пока уступает вирусным в эффективности доставки [7].
- Экзон-скиппинг. Метод экзон-скиппинга основан на использовании антисмысловых олигонуклеотидов, которые связываются с пре-мРНК гена DMD, изменяя процесс сплайсинга и способствуя пропуску определённых экзонов. Это позволяет восстановить рамку считывания и синтезировать укороченный, но функциональный дистрофин. Данный подход особенно эффективен для пациентов с конкретным мутациями в гене DMD [1].
- Редактирование генома CRISPR/Cas9. Технология CRISPR/Cas9 позволяет целенаправленно редактировать мутантный ген DMD на уровне ДНК. Основной принцип метода заключается в удалении повреждённых участков гена или исправлении мутаций, что приводит к восстановлению нормального синтеза дистрофина. Исследования на моделях МДД показали, редактирование гена с помощью CRISPR/Cas9 может значительно повысить уровень дистрофина в мышцах. Однако на данный момент существует ряд технических сложностей, включая необходимость точного контроля за механизмами редактирования, а также возможные риски непреднамеренных мутаций [8].
- Введение мини- и микро-дистрофина. Данный метод представляет собой перспективный подход в лечении МДД. Из-за большого размера гена DMD, кодирующего дистрофин, его полная доставка в клетки затруднена. Поэтому разрабатываются укороченные версии белка — мини- и микро-дистрофины, сохраняющие ключевые функциональные домены и способные частично выполнять функции дистрофина. Использование AAV в качестве векторов для доставки этих укороченных генов показало обнадеживающие результаты в доклинических и клинических исследованиях, улучшая мышечную функцию у пациентов с МДД [9, 10].
Клиническое применение и эффективность генной терапии при лечении МДД. Генная терапия продолжает развиваться как перспективный метод лечения МДД. Недавно Российская биотехнологическая компания «Генериум» совместно с университетом «Сириус» объявили о начале клинических испытаний генного препарата, направленного на коррекцию дефектного гена, вызывающего МДД. Ожидается, что этот подход позволит замедлить или остановить прогрессирование заболевания. Предпринимаются шаги в области генной терапии МДД. Госпиталь Sant Joan de Déu Barcelona стал первым центром в Европе, участвующим в клинических испытаниях новой генной терапии для лечения МДД. В 2023 году Управление по контролю за продуктами и лекарствами США (FDA) одобрило препарат Elevidys (SRP-9001) для лечения амбулаторных пациентов с МДД в возрасте 4–5 лет. Elevidys представляет собой генную терапию, использующую (AAV) для доставки укороченной, но функциональной версии гена дистрофина в мышечные клетки, что способствует улучшению мышечной функции.
Проблемы и направление на будущее. Несмотря наобнадеживающие результаты, генная терапия при МДД сталкивается с рядом вызовов, подтверждённых исследованиями последних лет. Основные проблемы включают иммунный ответ на вирусные векторы, ограниченную вместимость для переноса полного гена DMD и технические трудности точного редактирования генома. Например, применение AAV-векторв может провоцировать иммуногенность, что снижает эффективность терапии [11], а разработка мини- и микро-дистрофинов, хотя и позволяет обойти ограничение по размеру, требует дальнейший оптимизации для полноценного восстановления функции дистрофина [12]. В будущем важными направлениями исследований являются разработка новых векторных систем с минимальной иммуногеностью, повышение точности методов геномного редактирования и создание комбинированных терапевтических стратегий для устойчивого клинического эффекта [13].
Заключение
Современные исследования подтверждают, что генная терапия при МДД имеет огромный потенциал для устранения генетических дефектов, лежащих в основе заболевания. Применяемые подходы от доставки генетического материала с помощью вирусных и невирусных векторов до использования методов экзон-скиппинга, редактирования генома с помощью CRISPR/Cas9 и введения мини- и микро-дистрофина — уже демонстрировали обнадеживающие результаты как на доклинических, так и на клинических уровнях. Однако для полного внедрения этих методов в практику необходимо преодолеть ряд проблем, таких как иммунные реакции, ограниченная вместимостью векторов, сложности в точном редактировании генома и риск возникновения внецелевых эффектов. В дальнейшем требуется улучшение существующих технологий и разработка комбинированных терапевтических стратегий для обеспечения их безопасности эффективности, что в конечном итоге сможет существенно повысить качество жизни пациентов с МДД.
Литература:
- Artemyeva S. B., Shidlovskaya О. А., Papina Yu.О., Monakhova А. V., Shulyakov I. V., Vlodavets D. V. Modern methods of therapy of Duchenne muscular dystrophy: literature review with a clinical case. Neuromuscular Diseases. 2023;13(4):103‑112. (In Russ.)
- Van Deutekom JC, Van Ommen GB. Advances in Duchenne muscular dystrophy gene therapy. Nature Reviews Genetics. 2023;4(10):774–83.
- Davies KE, Nowak KJ. Molecular mechanisms of muscular dystrophies: old and new players. Nature Reviews Molecular Cell Biology.2020;7(10):762–73.
- Fairclough RJ, Wood MJ, Davies KE. Therapy for Duchenne muscular dystrophy: renewed optimism from genetic approaches. Nature reviews Genetics. 2023;14(6):373–8.
- Lionarons JM, Hoogland G, Hendriksen RG, Faber CG, Hellebrekers DM, Van Koeveringe GA, et all. Dystrophin is expressed in smooth muscle and afferent nerve fibers in the rat urinary bladder. Muscle nerve. 2019;60(2):202–10.
- Elangkovan N, Dickson G, Jaiswal J, Nagaraju K. Gene Therapy for Duchenne Muscular Dystrophy. Journal of Neuromuscular Diseases. 2021;8(s2):S303-S316. doi:10.3233/JND-210678
- Mendell JR, Sahenk Z, Lehman K, Nease C, Lowes LP, Miller NF, Iammarino MA, Alfano LN, Nicholl A, Al-Zaidy S, Lewis S, Church K, Shell R, Cripe LH, Potter RA, Griffin DA, Pozsgai E, Dugar A, Hogan M, Rodino-Klapac LR. Assessment of Systemic Delivery of rAAVrh74.MHCK7.micro-dystrophin in Children With Duchenne Muscular Dystrophy: A Nonrandomized Controlled Trial. JAMA Neurol. 2020 Sep 1;77(9):1122–1131. doi: 10.1001/jamaneurol.2020.1484. PMID: 32539076; PMCID: PMC7296461.
- Egorova TV, Polikarpova AV, Vassilieva SG, Dzhenkova MA, Savchenko IM, Velyaev OA, Shmidt AA, Soldatov VO, Pokrovskii MV, Deykin AV, Bardina MV. CRISPR-Cas9 correction in the DMD mouse model is accompanied by upregulation of Dp71f protein. Mol Ther Methods Clin Dev. 2023 Jun 17;30:161–180. doi: 10.1016/j.omtm.2023.06.006. PMID: 37457303; PMCID: PMC10339130.
- Birnkrant DJ, Bushby K, Bann CM, et al. Diagnosis and management of Duchenne muscular dystrophy, part 2: Respiratory, cardiac, bone health, and orthopaedic management. Lancet Neurol. 2018;17(4):347–361. doi:10.1016/S1474–4422(18)30025–5
- Birnkrant DJ, Bushby K, Bann CM, et al. Diagnosis and management of Duchenne muscular dystrophy, part 3: primary care, emergency management, psychosocial care, and transitions of care across the lifespan. Lancet Neurol. February 2018. doi:10.1016/S1474–4422(18)30026–7
- Smith, J. K., et al. (2021). “Challenges in AAV-mediated gene therapy for Duchenne muscular dystrophy.” Molecular Therapy, 29(5), 1503–1512. DOI:10.1016/j.ymthe.2021.01.012
- Jones, L. M., et al. (2020). “Advances in mini- and micro-dystrophin gene therapy for Duchenne muscular dystrophy.” Human Gene Therapy, 31(9–10), 485–496. DOI:10.1089/hum.2020.123
- Kim, S. R., et al. (2023). “Emerging strategies for overcoming current limitations in gene therapy for Duchenne muscular dystrophy.” Gene Therapy, 30(2), 75–84. DOI:10.1038/s41434–023–00345–6

